前文中,我们介绍了第三代芳香化酶抑制剂(AI),它可以与芳香化酶结合,引起体内雌激素水平的降低。那么这期,我们延续关于雌激素的问题,详细讲解乳腺癌卵巢功能抑制药物辅助治疗。

方医生专栏,知其所以然!
卵巢功能抑制(OFS)
卵巢功能抑制(OFS)是指通过手术、放疗或药物抑制卵巢产生雌激素。
乳腺癌使用OFS的目的是通过降低体内以及癌组织中的雌激素水平,抑制乳腺癌细胞的分裂增殖,从而达到控制乳腺癌的目的。
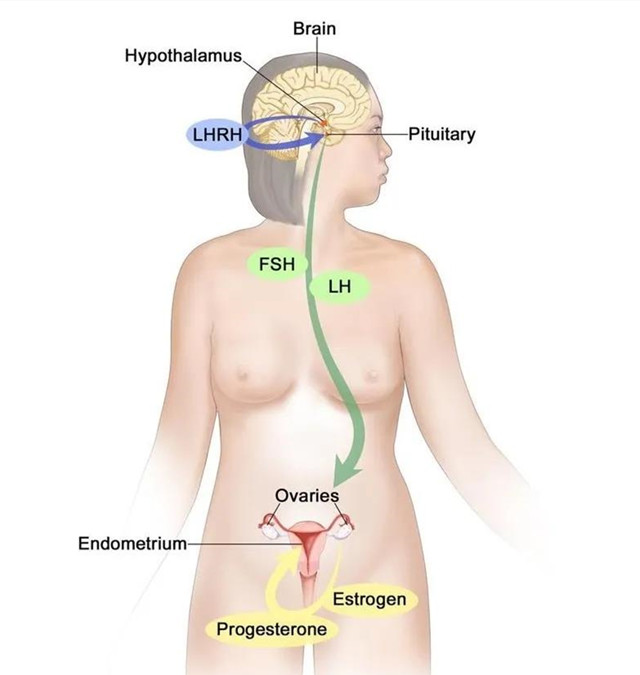
图片来源:cancer.gov
卵巢分泌雌激素受垂体产生的促卵泡激素(FSH)和促黄体激素(LH)的调控,后者的产生又受下丘脑分泌的促性腺激素释放激素(GnRH,也称黄体生成素释放激素LHRH)的控制。
GnRH激动剂(GnRHa,也称LHRHa)可以与垂体细胞膜上相应受体结合,一方面可负反馈抑制下丘脑产生GnRH,另一方面又可直接抑制垂体FSH和LH分泌,使绝经前女性的雌激素水平下降到绝经后的水平。
# GnRHa 常见药物:戈舍瑞林、曲普瑞林和亮丙瑞林。
现今,药物性OFS已成为绝经前ER阳性乳腺癌内分泌治疗的重要手段。接下来,我们从历史出发,一起回顾药物性OFS重要的辅助治疗临床研究。
OFS的临床研究
为比较戈舍瑞林与环磷酰胺和氨甲蝶呤加氟尿嘧啶(CMF)方案的疗效与安全性。
ZEBRA研究纳入1990-1996年共1614例淋巴结阳性绝经前早期乳腺癌患者,随机分成2组:
◎ 2年戈舍瑞林(3.6mg,每28天),6个疗程CMF(C:500mg/m²,第1、8天静脉滴注。
◎ 100 mg/m²,第1-14口服;M:40 mg/m²;F:600mg/m²,每28天为一个疗程)。
# 研究结果显示:对于ER阳性患者,两组的无病生存(DFS)和总生存(OS)无显著差异。
但对于ER阴性患者,戈舍瑞林组的DFS较CMF组差。戈舍瑞林组相比CMF组,在6个月内闭经的发生率(>95%对比58.6%)以及治疗结束后月经恢复率更高(3年后无月经率22.6%对比76.9%)。不良反应如恶心、呕吐、脱发等在CMF组更多见。
ZEBRA研究结果表明对于ER阳性淋巴结阳性的绝经前早期乳腺癌患者,戈舍瑞林与CMF化疗疗效相当,并戈舍瑞林耐受性更佳。
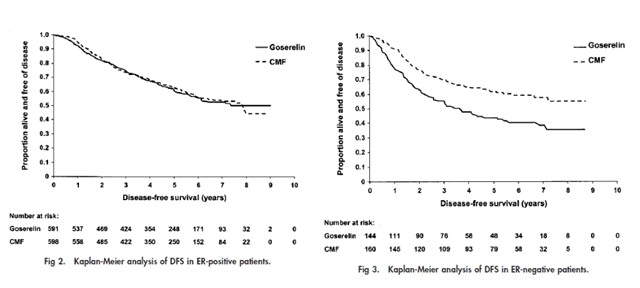
图片来源:Jonat W, et al. J Clin Oncol, 2002,20(24):4628-4635.
OFS+TAM的临床研究
进一步,为探索戈舍瑞林联合他莫昔芬(TAM)与标准化疗辅助治疗的疗效,Raimund Jakesz等人的ABCSG 5研究纳入了1990-1999年共1034例激素受体阳性的绝经前早期乳腺癌患者,随机分成两组:
◎ 戈舍瑞林(3.6mg,每28天,3年)+5年TAM。
◎ 6个疗程CMF(C:600mg/m²;M:40 mg/m²;F:600mg/m²)。

Raimund Jakesz
图片来源:suzystoeckl.com
# 中位随访60个月结果显示:
戈舍瑞林+TAM组与CMF组的复发率分别为17.2%和20.8%,局部复发率分别为4.7%和8%,戈舍瑞林+TAM组的无复发率和无局部复发生存率均优于CMF组(P=0.037,P=0.015),OS也有相同的趋势(P=0.195)。
该试验表明在激素受体阳性的绝经前早期乳腺癌患者的辅助治疗中,戈舍瑞林+TAM使用比CMF化疗更加有效。
2007年,英国Cuzick等人发表了一项对16项随机对照试验(包含上述ZEBRA和ABCSG 5两个研究)共11906患者的Meta分析,观察GnRHa治疗对绝经前早期乳腺癌患者复发和死亡的影响。
# 研究结果显示 #
激素受体阳性患者GnRHa单药(多数研究GnRHa为戈舍瑞林)与化疗的疗程获益相似,复发率(P=0.08)和复发后病死率(P=0.49)无显著降低。GnRHa+TAM联用则可降低复发率(P=0.02)以及复发后病死率(P=0.03)。GnRHa对激素受体阴性患者无效。
该研究进一步证实了GnRHa可用于绝经前激素受体阳性乳腺癌患者的治疗。
OFS+TAM与OFS+AI的临床研究
# 2014年Prudence Francis等人公布了SOFT研究的5年随访结果:
OFS+TAM对比TAM单药在总体人群没有显著获益。但在接受化疗的亚组中,与TAM单药对比,OFS+芳香化酶抑制剂(AI)和OFS+TAM的5年无乳腺癌生存绝对获益分别为7.7%和4.5%,复发风险分别降低35%和22%;年龄<35岁亚组中,与TAM单药对比,OFS+AI和OFS+TAM的5年无乳腺癌生存绝对获益分别为15.7%和11.2%。

Prudence Francis
图片来源:emedevents.com
这一研究结果确立了OFS+TAM/AI在早期激素受体阳性中高危乳腺癌中的标准治疗地位。
# 而SOFT研究8年随访结果更颠覆了之前整体人群阴性的结论,证实了OFS+TAM/AI能显著改善绝经前激素受体阳性早期乳腺癌整体人群的DFS。
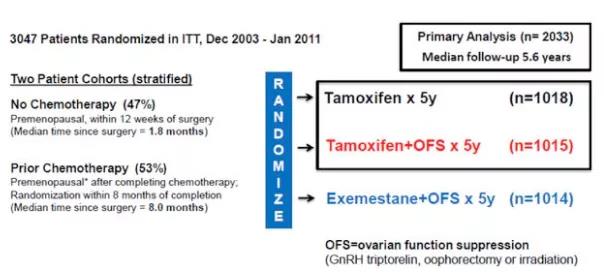
图片来源:slidetodoc.com
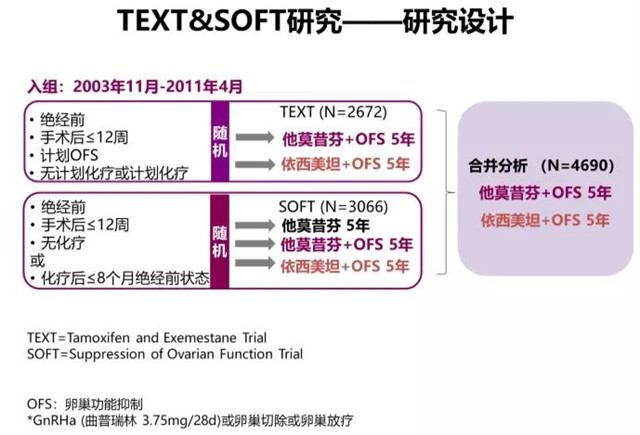
# 2014年,发表了大型临床试验SOFT、TEXT研究的联合分析结果:
OFS+AI对比TAM单药,在低复发风险患者中,5年无乳腺癌生存效果近似;在中复发风险患者中,5年无乳腺癌生存绝对获益>5%;在高复发风险患者中,5年无乳腺癌生存达到10%-15%。
研究证明了OFS的获益在高复发风险患者中较为显著。因此,2015年St. Gallen共识指出,考虑使用OFS的因素包括:
● 年龄≤35
● 接受辅助化疗后仍为绝经前
● 4个淋巴结转移
● 组织学分级为3级
● 或多基因检测显示不良预后的患者
图片来源:new.qq.com
# 8年的随访联合分析结果 #
2017年,研究公布了8年的随访联合分析结果,显示相比OFS+TAM组,OFS+AI组显著改善8年DFS、无乳腺癌间期以及无远处复发间期。在安全性事件上,两组无明显差异。
在TEXT研究中,安全性事件两组无明显差异,潮热、肌肉骨骼症状和高血压是最常见的3-4级不良反应。
在SOFT研究中,OFS+TAM的不良反应发生率略高于TAM单药组,3级以上的不良反应的风险分别为32%和25%。
SOFT、TEXT联合分析证实了相较于OFS + TAM,OFS+AI能够持续减少复发风险。
结语
1896年,英国学者Beaton首次通过切除双侧卵巢治疗晚期乳腺癌,揭开了乳腺癌内分泌治疗的序幕。距今,内分泌治疗已经历了100多年的历史,已成为乳腺癌全身治疗的重要方法之一。
OFS联合内分泌药物的使用适用于绝经前、复发风险较高的乳腺癌患者,能进一步提高治疗的效果。
附言:由于篇幅关系,当中还有许多OFS重要的辅助治疗临床研究未能详细介绍。
参考文献
[1] 邵志敏,沈镇宇,徐兵河. 乳腺肿瘤学[M].上海:复旦大学出版社,2018.
[2] Jonat W, et al. J Clin Oncol, 2002,20(24):4628-4635.
[3] Jakesz R, et al. J Clin Oncol, 2002,20(24):4621-4627.
[4] Cuzick J,et al. Lancet, 2007,369(9574):1711-1723.
[5] Francis PA, et al. N Engl J Med, 2015,372(5):436-446.
[6] Pagani O, et al. N Engl J Med, 2014,371(2):107-118.
[7] Saha P, et al. J Clin Oncol, 2017,35(27):3113-3122.
本期卵巢功能抑制药物,您有什么收获与感想?
欢迎在留言区与我们分享交流哦~
-本文为原创作品,转载须得授权,侵权必究-
方医生|撰文
尤秋婷医生|审核
常钰滢|排版
 标签来源:卵巢功能抑制
标签来源:卵巢功能抑制